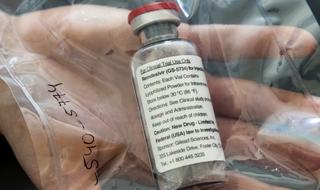
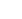Hasta que se encuentre una vacuna contra el COVID-19, uno de los principales desafíos de la humanidad es encontrar un antiviral efectivo y una de las drogas más prometedoras es el Remdesivir.
Desarrollado originalmente para combatir el virus del ébola durante un gran brote que afectó a África en 2014. Y esta es su gran ventaja respecto a otras investigaciones que se realizan en plena pandemia, ya que su antigüedad esquiva muchas etapas necesarias para obtener la aprobación de las autoridades de salud de cada país. ¿Pero es acaso el Remdesivir la solución definitiva para el coronavirus?
Esta droga ya se encuentra en una fase de ensayos clínicos y los primeros pacientes en recibir este tratamiento fueron pasajeros del crucero Diamond Princess, uno de los primeros focos de COVID-19 que tuvo repercusión internacional y registró más de 700 casos de contagio.
2 צפייה בגלריה


El antiviral Remdesivir comenzó a experimentarse en el crucero Diamond Princess.
(AFP)
Para evaluar la eficacia del Remdesivir los pacientes voluntarios fueron divididos en dos grupos: a uno se le suministró la droga y a otro placebo. El ensayo duró 15 días y se tabuló la evolución de cada paciente al final del período en una escala del 1 al 8, en la cual 1 significaba que el paciente había muerto y 8 una total recuperación de la persona.
El procesamiento de los datos obtenidos pareció suficiente para evaluar la seguridad y eficacia de la droga. Pero como el experimento se hizo sobre un bajo número de participantes desde el Instituto Nacional de Salud (NIH) de Estados Unidos, organismo a cargo del proyecto, se resolvió cambiar la hipótesis por temor a emitir resultados sesgados: en lugar de establecer si el Remdesivir salvaba vidas, emitieron conclusiones sobre la capacidad del medicamento en acortar la duración de la enfermedad. En función de esa nueva hipótesis, y con un 6 de promedio en la escala establecida, se concluyó que los pacientes tratados con Remdesivir atravesaron una recuperación más corta que aquellos que recibieron placebo.
A raíz de este cambio en la hipótesis del experimento, el siguiente paso de la NIH fue repetir el ensayo pero esta vez de manera extendida, con 1.063 pacientes voluntarios. Además, se convocó a un comité externo para que revisara el proceso de análisis de datos, los resultados del estudio y la seguridad del medicamento. La evaluación del comité fue positiva y tras la recuperación de 480 de los 1063 casos realizó una serie de recomendaciones: interrumpir el ensayo e iniciar una nueva instancia de investigación que comparara los efectos del Remdesivir con los de otro medicamento, llamado Olumiant, sin la necesidad de un grupo de control que recibiera placebo.
El NIH aceptó la recomendación de suspender el uso de placebo, aunque las opiniones en la comunidad científica están divididas respecto a esta decisión: los opositores sostienen que el objetivo de desarrollar un medicamento contra el COVID-19 es prevenir la muerte y no acortar la duración de la enfermedad, y que suspender la investigación en grupos de control por la recuperación de 480 pacientes sobre 1063 afecta a la capacidad de deducir si la droga contribuye a las posibilidades de supervivencia real de los pacientes.
2 צפייה בגלריה
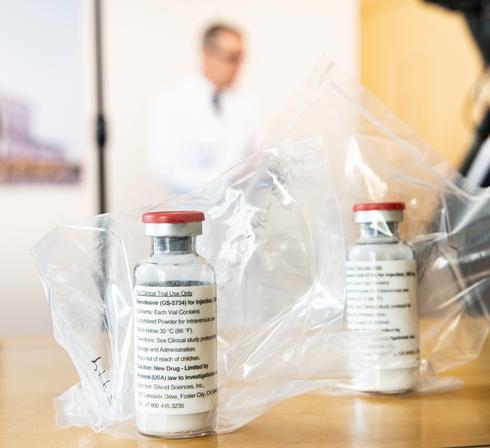

El proceso de experimentación del Remdesivir despertó controversias en la comunidad científica.
(Reuters)
Los resultados preliminares de ese controvertido estudio determinaron que, hasta el momento de la interrupción del experimento, el Remdesivir redujo la tasa de mortalidad del 11,6% al 8%. Pero un análisis estadístico, que contempla no solo las tasas de mortalidad sino también el alcance de la muestra, asegura que esa diferencia no es significativa para cumplir con los estándares de investigación que exigen superar el 95% de confiabilidad. Los opositores al NIH argumentan que si el estudio original no se hubiera detenido, la cantidad de casos en el muestreo hubiera sido más grande y la comunidad médica hoy tendría mejores herramientas para sacar conclusiones sobre la capacidad del Remdesivir para salvar vidas.
Quienes defienden la postura del NIH sostienen un argumento ético: afirman que en cuanto se demostró que el Remdesivir era un medicamento efectivo y capaz de salvar vidas, correspondía suspender el suministro de placebos para favorecer las posibilidades de recuperación de los pacientes que recibían esta falsa medicación. Además, sostienen que si bien no se alcanzó el estándar científico del 95%, en un contexto de pandemia el 81% logrado fue suficiente para priorizar la salud de esos voluntarios.
La FDA, organismo que regula la utilización de medicamentos en Estados Unidos, aprobó al Remdesivir solamente como un medicamento de emergencia, aunque eso no impidió que el laboratorio que lo produce lo comercializara en 127 países. Por el momento los acuerdos no incluyen regalías y esto continuará así hasta que el COVID-19 deje de ser considerado pandemia, o hasta que las autoridades sanitarias aprueben una nueva droga.